Erhöhte Entzündungswerte im ganzen Körper durch Parodontitis
Eine Parodontitis spielt sich nicht nur im Mund ab. Die chronische Entzündung hinterlässt Spuren im ganzen Körper – und die lassen sich im Blut messen. Das ist keine theoretische Überlegung, sondern harte Labordiagnostik: Mehrere Entzündungsmarker sind bei Parodontitis-Patienten signifikant erhöht. Diese Werte zeigen, dass der gesamte Organismus auf die Entzündung im Mund reagiert.
Für Ärzte und Patienten hat das praktische Bedeutung: Erhöhte Entzündungswerte bei ansonsten unerklärlicher Ursache sollten an eine Parodontitis denken lassen. Und umgekehrt: Eine erfolgreiche Parodontitis-Behandlung senkt diese Werte messbar.
CRP: der wichtigste Entzündungsmarker
Herzinfarktrisiko steigt
Das C-reaktive Protein (CRP) ist der am häufigsten bestimmte Entzündungsmarker im klinischen Alltag. Die Leber bildet CRP als Antwort auf Entzündungsprozesse im Körper – egal wo diese stattfinden. Kardiologen nutzen das hochsensitive CRP (hs-CRP) seit Jahren zur Einschätzung des Herzinfarkt-Risikos. Die American Heart Association definiert klare Grenzwerte:
| CRP-Wert | Kardiovaskuläres Risiko |
|---|---|
| unter 1 mg/L | Niedriges Risiko |
| 1–3 mg/L | Mittleres Risiko |
| über 3 mg/L | Hohes Risiko |
Bei Menschen mit gesundem Zahnfleisch liegt der CRP-Wert typischerweise unter 1 mg/L – also im niedrigen Risikobereich. Mit zunehmendem Schweregrad der Parodontitis steigt das CRP stufenweise an: Schon eine Gingivitis kann den Wert in den mittleren Risikobereich verschieben. Bei mittelschwerer bis schwerer Parodontitis liegt das CRP häufig über 3 mg/L und damit im Bereich „hohes kardiovaskuläres Risiko“. In Studien wurden bei schwerer Parodontitis CRP-Werte gemessen, die den Normalwert um das 5- bis 8-Fache übersteigen.
Diese Zahlen verdeutlichen: Eine Parodontitis ist eine systemische Entzündung, nicht nur ein lokales Problem im Mund.
Auch andere Entzündungsmarker bei Parodontitis erhöht
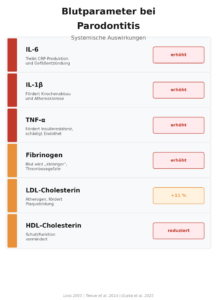
CRP ist der bekannteste, aber nicht der einzige Laborwert, der bei Parodontitis verändert ist. Das Bild wird vollständiger, wenn man weitere Marker betrachtet:
Interleukin-6 (IL-6) ist einer der Haupttreiber der systemischen Entzündungsreaktion. IL-6 wird direkt im entzündeten Zahnfleisch produziert und gelangt über die Blutbahn in den gesamten Körper. In der Leber stimuliert IL-6 die CRP-Produktion – es ist also der Botenstoff, der die CRP-Erhöhung auslöst. Bei Parodontitis-Patienten sind die IL-6-Spiegel im Blut deutlich erhöht.
Interleukin-1β (IL-1β) ist ein weiterer zentraler Entzündungsbotenstoff. Er fördert direkt den Knochenabbau im Kiefer und treibt gleichzeitig die Atherosklerose in den Blutgefäßen voran. IL-1β ist bei Parodontitis-Patienten sowohl lokal im Zahnfleisch als auch systemisch im Blut erhöht. Dass dieser Botenstoff klinisch relevant ist, zeigt die CANTOS-Studie (2017): Allein die Hemmung von IL-1β senkte das Herzinfarktrisiko – ohne Cholesterinsenkung, ohne Blutdruckbehandlung.
TNF-alpha (Tumornekrosefaktor alpha) ist ein weiterer Entzündungsbotenstoff, der bei Parodontitis vermehrt ausgeschüttet wird. TNF-alpha spielt eine zentrale Rolle bei der Insulinresistenz – er ist damit ein wichtiges Bindeglied zwischen Parodontitis und Diabetes. Gleichzeitig fördert er den Knochenabbau, sowohl im Kiefer als auch im übrigen Skelett.
Fibrinogen ist ein Gerinnungsfaktor. Erhöhte Fibrinogenwerte machen das Blut „klebriger“ und erhöhen damit das Risiko für Blutgerinnsel. Bei Parodontitis-Patienten ist Fibrinogen signifikant erhöht – ein weiterer Mechanismus, über den die Mundentzündung das Herzinfarkt- und Schlaganfall-Risiko steigert.
Leukozyten (weiße Blutkörperchen) sind bei Parodontitis oft leicht erhöht. Das ist die direkte Antwort des Immunsystems auf die chronische Infektion. Die Leukozytose ist meist mild, aber messbar.
Matrix-Metalloproteinasen (MMPs), insbesondere MMP-8 und MMP-9, sind bei Parodontitis-Patienten im Blut erhöht. Diese Enzyme bauen Bindegewebe ab – im Mund zerstören sie den Zahnhalteapparat, systemisch können sie zur Destabilisierung von Gefäßplaques beitragen.
Interleukin-8 (IL-8) nimmt eine Sonderstellung ein: Es ist vor allem in der Sulkusflüssigkeit – also direkt in der Zahnfleischtasche – massiv erhöht und gilt dort als einer der wichtigsten Parodontitis-Marker überhaupt. IL-8 lockt Immunzellen gezielt an den Entzündungsort und spielt eine Schlüsselrolle bei der lokalen Gewebezerstörung. Im Blut ist IL-8 weniger zuverlässig nachweisbar als IL-6 oder TNF-α, seine klinische Bedeutung liegt primär in der lokalen Entzündungsdiagnostik.
| Marker | Funktion | Veränderung bei Parodontitis |
|---|---|---|
| CRP | Allgemeiner Entzündungsmarker | 5- bis 8-fach erhöht |
| Interleukin-6 (IL-6) | Entzündungsbotenstoff, treibt CRP-Produktion | Deutlich erhöht |
| Interleukin-1β (IL-1β) | Entzündungsbotenstoff, fördert Knochenabbau und Atherosklerose | Erhöht |
| TNF-alpha | Entzündungsbotenstoff, fördert Insulinresistenz | Erhöht |
| Fibrinogen | Gerinnungsfaktor | Erhöht |
| Leukozyten | Weiße Blutkörperchen | Leicht erhöht |
| MMP-8, MMP-9 | Gewebeabbauende Enzyme | Erhöht |
| Interleukin-8 (IL-8) | Immunzell-Lockstoff | Vor allem lokal in der Zahnfleischtasche stark erhöht |
Lipidprofil: auch die Blutfette entwickeln sich ungünstig
Neben den Entzündungsmarkern beeinflusst Parodontitis auch das Lipidprofil: LDL-Cholesterin („schlechtes“ Cholesterin) ist bei Parodontitis-Patienten erhöht, HDL-Cholesterin („gutes“ Cholesterin) signifikant reduziert. Die chronische Entzündung fördert zudem die Oxidation von LDL-Partikeln – ein erster Schritt der Atherosklerose. Mehr dazu im Kapitel Parodontitis und Herz-Kreislauf-Erkrankungen.
Handeln für Patient und Arzt erforderlich
Die erhöhten Entzündungswerte bei Zahnbettentzündungen sind mehr als ein akademisches Detail. Sie haben konkrete klinische Konsequenzen.
Für Ärzte: Wenn ein Patient dauerhaft erhöhte CRP-Werte zeigt und keine offensichtliche Ursache gefunden wird – keine Infektion, keine Autoimmunerkrankung, kein Tumor – sollte an eine Parodontitis gedacht werden. Ein Blick in den Mund oder die Überweisung zum Zahnarzt kann die Lösung sein. Das gilt besonders für Kardiologen, die das hs-CRP zur Risikostratifizierung nutzen: Ein Teil der „unerklärten“ CRP-Erhöhung kann aus dem Mund stammen.
Für Patienten: Wer bei einer Blutuntersuchung erhöhte Entzündungswerte aufweist, sollte auch an sein Zahnfleisch denken. Das gilt besonders, wenn gleichzeitig Zahnfleischbluten oder andere Parodontitis-Symptome bestehen.
Parodontose-Behandlung normalisiert Entzündungswerte
Studien zeigen konsistent: Eine erfolgreiche Parodontitis-Behandlung senkt die Entzündungswerte im Blut messbar. Nach einer systematischen Parodontaltherapie normalisieren sich CRP und andere Marker oft innerhalb weniger Wochen. Die Reduktion ist klinisch relevant – sie verschiebt Patienten von „hohem“ zurück in „niedriges“ oder „mittleres“ kardiovaskuläres Risiko.
Oxidativer Stress bei Zahnfleischentzündung
Neben den klassischen Entzündungsmarkern ist auch der oxidative Stress bei Parodontitis erhöht. Reaktive Sauerstoffspezies (ROS) – aggressive Moleküle, die Zellen und Gewebe schädigen – werden bei chronischer Entzündung vermehrt gebildet. Bei Parodontitis ist das antioxidative Schutzsystem des Körpers überfordert: Die Balance zwischen schädlichen ROS und schützenden Antioxidantien verschiebt sich zugunsten der ROS.
Oxidativer Stress spielt eine Rolle bei nahezu allen Erkrankungen, die mit Parodontitis in Verbindung gebracht werden: Atherosklerose, Diabetes, Alzheimer, erektile Dysfunktion. Er ist damit ein übergeordneter Mechanismus, der die verschiedenen Krankheitszusammenhänge verbindet.
implantate.com-Fazit:
Die Entzündungswerte im Blut sind der objektivste Beweis dafür, dass Parodontitis keine lokale Angelegenheit ist. Ein CRP, das den Normalwert um das 5- bis 8-Fache übersteigt, erhöhte Gerinnungsfaktoren, systemischer oxidativer Stress – das sind keine Zufallsbefunde, sondern messbare Folgen einer chronischen Infektion im Mund.
Wenn Sie als Patient dauerhaft erhöhte Entzündungswerten im Blut haben, lohnt sich der Blick in den Mund. Erfolgreiche Parodontitis-Behandlung normalisiert die Werte: ein gesundheitlicher Erfolg für den ganzen Körper.
Amar S, Gokce N, Morgan S et al.: Periodontal disease is associated with brachial artery endothelial dysfunction and systemic inflammation. Arterioscler Thromb Vasc Biol 2003;23(7):1245–1249.
Ridker PM: C-Reactive Protein and the Prediction of Cardiovascular Events Among Those at Intermediate Risk. J Am Coll Cardiol 2007;49(21):2129–2138.
Ridker PM, Everett BM, Thuren T et al.: Antiinflammatory Therapy with Canakinumab for Atherosclerotic Disease (CANTOS). N Engl J Med 2017;377(12):1119–1131.
Konkel JE, O’Boyle C, Krishnan S: Distal Consequences of Oral Inflammation. Front Immunol 2019;10:1403.