Bakterientest auf Markerkeime bei Parodontitis
Warum, was passiert – und was kostet er?
Welche Bakterien sich in Ihren Zahnfleischtaschen eingenistet haben, entscheidet darüber, wie aggressiv die Erkrankung verläuft – und ob eine mechanische Parodontose-Behandlung allein ausreicht oder ein Antibiotikum gezielt eingesetzt werden sollte. Genau das leistet der Bakterientest: Er macht die unsichtbaren Gegner sichtbar und sagt auch, wie man sie am besten bekämpft
Auf einen Blick
| Was ist das? | Molekularbiologische Analyse der Bakterien in Ihren Zahnfleischtaschen – meist per PCR (Polymerasekettenreaktion) |
| Für wen sinnvoll? | Bei schwerem oder schnell fortschreitendem Verlauf, vor Antibiotikaentscheidung, bei Rückfällen nach Behandlung |
| Ablauf | Sterile Papierspitze wird einige Sekunden in die tiefste Tasche eingeführt – schmerzlos |
| Ergebnis | Welche Markerkeime in welcher Konzentration vorhanden sind (oft 5 oder 11 Bakterienarten) |
| Kosten | 45 bis 200 Euro, je nach Testumfang |
| Kassenerstattung | keine Kassenleistung! Die meisten PKV-Tarife und Zusatzversicherungen beteiligen sich |
Brauche ich überhaupt einen Bakterientest bei Parodontose?
Der Zahnarzt sieht bei der Untersuchung, wie tief die Zahnfleischtaschen sind und ob es blutet. Was er bei einer schweren Erkrankung nicht sehen kann: Welche der mehr als 700 bekannten Bakterienarten der Mundflora dort aktiv sind – und ob darunter besonders aggressive und hartnäckige Markerkeime sind, die besser mit einer zusätzlichen Antbiotikagabe zur Parodontosebehandlung eliminiert werden können.
Das ist klinisch relevant, weil bestimmte Parodontitis-Erreger sehr unterschiedlich auf Behandlung ansprechen:
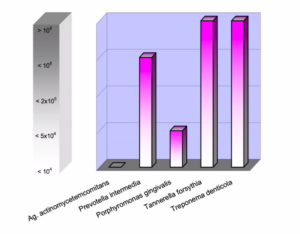
- Porphyromonas gingivalis, Treponema denticola und Tannerella forsythia (der sogenannte rote Komplex) reagieren gut auf mechanische Reinigung der Wurzeloberflächen – sofern die Taschen vollständig gesäubert werden.
- Aggregatibacter actinomycetemcomitans (A.a.) hingegen kann tief ins Gewebe eindringen und ist durch alleiniges Scaling kaum zu eliminieren. Sein Nachweis ist die stärkste Indikation für ein systemisches Antibiotikum.
- Prevotella intermedia und andere anaerobe Keime sind bei bestehenden Systemerkrankungen wie Diabetes oder in der Schwangerschaft besonders relevant.
Kurz gesagt: Ohne Keimnachweis kann der Zahnarzt nicht immer zielgerichtet behandeln.
Wann ist ein Bakteriennachweis sinnvoll?
Nicht jeder Parodontitis-Patient braucht diesen Test. Die S3-Leitlinie der Deutschen Gesellschaft für Parodontologie (DG PARO) benennt klare Indikationen:
- Schwere oder rasch fortschreitende Parodontitis (Stadium III/IV, Grad C)
- Junge Patienten mit ausgeprägtem Attachmentverlust
- Erkrankung, die trotz vorangegangener Behandlung fortschreitet (refraktäre Parodontitis)
- Geplante Antibiotikabehandlung – zur gezielten Auswahl des Wirkstoffs
- Patienten mit Diabetes, Immunsuppression oder anderen systemischen Erkrankungen
- Therapiekontrolle nach der Behandlung
Routine-Screening bei milder Parodontitis ohne Risikofaktoren ist dagegen nicht erforderlich. Der Test ist ein Präzisionsinstrument – kein Standardprogramm.
|
PCR-Test: keine lebenden Bakterien für den Nachweis nötig
Das heute am häufigsten eingesetzte Verfahren ist die Polymerasekettenreaktion – kurz PCR. Viele kennen den Begriff aus der Corona-Pandemie; das Grundprinzip ist dasselbe: Spezifische DNA-Abschnitte werden vervielfältigt und nachgewiesen.
Wie PCR im Bakterientest funktioniert
Das Labor isoliert die DNA aus dem entnommenen Probenmaterial. Dann werden spezifische Abschnitte der Erbsubstanz einzelner Bakterienarten vervielfältigt – das ist das „C“ in PCR: Chain Reaction, Kettenreaktion. Selbst kleinste Mengen sind nachweisbar. Moderne Labors arbeiten häufig mit Real-Time-PCR (RT-PCR), die nicht nur das Vorhandensein eines Keims feststellt, sondern auch seine Konzentration quantifiziert.
Was PCR gegenüber älteren Verfahren auszeichnet:
- Keine lebenden Keime nötig: PCR weist DNA nach, nicht Stoffwechselaktivität. Anaerobe Bakterien, die auf dem Transportweg absterben würden, werden trotzdem zuverlässig erkannt.
- Hohe Empfindlichkeit: Schon ab etwa 100 Keimen in der Probe ist ein zuverlässiger Nachweis möglich.
- Schnell und standardisiert: Ergebnisse liegen meist innerhalb weniger Werktage vor.
Andere Verfahren wie ELISA, Immunfluoreszenz oder klassische Kulturen sind zwar weiterhin im Einsatz, aber PCR hat sich als Goldstandard in der parodontologischen Diagnostik etabliert.
Welche Parodontitis-Keime entdeckt der PCR-Test?
Das hängt vom gewählten Testprodukt ab. Der weit verbreitete micro-IDent-Test von Hain Lifescience gibt es in zwei Varianten: Der Basistest analysiert die 5 wichtigsten Parodontitis-Bakterien; die Erweiterung (micro-IDent plus) deckt 11 Markerkeime ab. Wichtig ist, dass zumindest die Keime des roten Komplexes (P. gingivalis, T. denticola, T. forsythia) und A. actinomycetemcomitans erfasst werden, da diese den größten klinischen Entscheidungswert haben.
Die Probenentnahme im Mund tut nicht weh
Der Eingriff ist einfach, vollständig schmerzlos und dauert weniger als eine Minute:
- Trockenlegung: Der Zahnarzt trocknet den Entnahmebereich mit einer Watterolle, damit Speichel das Ergebnis nicht verdünnt.
- Probenentnahme: Eine sterile Papierspitze wird in die tiefste oder entzündlichste Tasche eingeführt und verbleibt dort einige Sekunden, bis dass erkennbar Flüssigkeit aus dem Zahnfach extrahiert wurde.
- Transport: Die Papierspitze kommt in ein kleines Transportröhrchen – entweder als Poolprobe (generalisierte Parodontitis) oder als Einzelstellenanalyse.
- Versand: Das Röhrchen wird ins Labor geschickt. Besondere Kühlung ist nicht nötig, da DNA stabil ist.
- Ergebnis: Liegt meist innerhalb von 3 bis 5 Werktagen vor.
Was kostet der Bakterientest – und wer zahlt?
| Leistung | Kosten (ca.) |
|---|---|
| Basistest (5 Markerkeime) | 45 – 80 Euro |
| Erweiterter Test (11 Markerkeime) | 80 – 150 Euro |
| Probenentnahme durch Zahnarzt | 6 – 15 Euro (zusätzlich, nach GOZ) |
Mehr über die Kosten einer Parodontosebehandlung.
Was das Ergebnis bedeutet – und was danach kommt
Ein positiver Befund auf Aggregatibacter actinomycetemcomitans ist in der Regel ein klares Signal: Die mechanische Therapie allein wird nicht ausreichen. In diesem Fall empfiehlt die S3-Leitlinie die adjuvante Antibiotkatherapie der Parodontitis von Amoxicillin und Metronidazol (sogenannter Van-Winkelhoff-Cocktail) – aber stets als Ergänzung zur mechanischen Reinigung, nie als Ersatz.
Werden nur Keime des roten Komplexes nachgewiesen – ohne A.a. –, reicht bei vielen Patienten eine konsequente Scaling-und-Root-Planing-Therapie aus. Das Ergebnis schützt dann vor unnötiger Antibiotikabehandlung.
Der Test kann auch nach der Parodontitis-Behandlung eingesetzt werden: als Erfolgskontrolle. Wenn therapieassoziierte Keime nach Abschluss der Parodontitistherapie noch immer in hoher Konzentration nachweisbar sind, ist eine Nachbehandlung indiziert – bevor klinische Zeichen erneut auftreten.
|
implantate.com-Fazit:
Wer eine leichte Parodontitis hat und keine Risikofaktoren, braucht keinen Bakterientest. Wer aber mit schwerem Verlauf, Rückfällen oder der Frage konfrontiert ist, ob ein Antibiotikum nötig ist, bekommt durch den Test eine klare Entscheidungsgrundlage.
Beikler T, Karch H, Flemmig TF: Mikrobiologische Diagnostik in der Parodontitistherapie – Gemeinsame Stellungnahme der Deutschen Gesellschaft für Parodontologie (DGP) und der Deutschen Gesellschaft für Zahn-, Mund- und Kieferheilkunde (DGZMK). DZZ 60 (2005) 12, S. 660–662.
Cosgarea R, Wenzel S, Jepsen K: Systemische Antibiotika in der Parodontaltherapie: Nutzen und Risiken. ZM 2022; 112:36–41.
Behandlungsrichtlinie zur systematischen Behandlung von Parodontitis und anderer Parodontalerkrankungen (PAR-Richtlinie). In Kraft seit 01.07.2021.
Deutsche Gesellschaft für Parodontologie (DG PARO): Die Behandlung von Parodontitis Stadium I bis III – Deutsche Implementierung der S3-Leitlinie der EFP. DG PARO/DGZMK, 02/2021.
Verantwortlicher Autor
Tätigkeitsschwerpunkt Implantologie, Spezialist für Parodontologie und Zahnersatz, Mitgliedschaften(u.a.), Deutsche Gesellschaft f. Zahn-, Mund- und Kieferheilkunde (DGZMK), Deutsche Gesellschaft f. Implantologie (DGI), Deutsche Gesellschaft f. Paodontologie (DGParo)