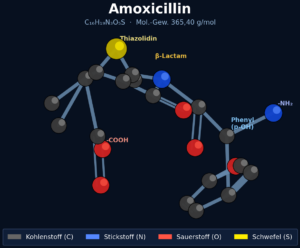
Amoxicillin zur Antibiotikatherapie der Parodontitis und Kiefererkrankungen
Amoxicillin ist weltweit das am häufigsten verordnete Antibiotikum – rund 30 Prozent aller Antibiotikaverordnungen in Deutschland entfallen auf diesen Wirkstoff. In der Parodontologie spielt Amoxicillin eine besondere Rolle: Als Partner von Metronidazol bildet es die erste Wahl der systemischen Antibiotikabehandlung bei schwerer Parodontitis. Auf der Liste der unentbehrlichen Arzneimittel der Weltgesundheitsorganisation steht es seit Jahrzehnten.
Was macht der Wirkstoff Amoxicillin in unserem Körper?
Amoxicillin kam 1972 kam es unter dem Handelsnamen Amoxil als Weiterentwicklung von Ampicillin, dem ersten oral wirksamen Breitbandpenicillin, auf den Markt.
Die orale Bioverfügbarkeit liegt Amoxicillin bei 70–90 Prozent gegenüber 30-40% bei Ampicillin. Das macht den Wirkstoff so erfolgreich, denn von einer Tablette kommt deutlich mehr Wirkstoff im Blut an – auch im entzündeten Zahnbett.
Wirkmechanismus: Amoxicillin bindet an sogenannte Penicillin-bindende Proteine (PBP) in der Bakterienzellwand. Diese Proteine sind für den Aufbau der Zellwand zuständig. Wird ihre Funktion blockiert, kann die Bakterienzelle keine stabile Wand mehr bilden – sie stirbt ab. Amoxicillin wirkt also bakterizid: Es tötet Bakterien, statt sie nur am Wachstum zu hindern.
Bei Parodontitis mit Metronidazol im Van-Winkelhoff-Cocktail hoch effizient
In der Parodontologie wird Amoxicillin nicht als Einzelpräparat eingesetzt. Es wird fast immer in Kombination mit Metronidazol – dem sogenannten Van-Winkelhoff-Cocktail (nach dem Mikrobiologen Arie Jan van Winkelhoff) eingesetzt..
Warum diese Kombination? Die Logik dahinter ist mikrobiologisch zwingend: Metronidazol wirkt hervorragend gegen strikt anaerobe Bakterien – also genau gegen die die Markerkeime des roten Komplexes wie Porphyromonas gingivalis (P.g.), Treponema denticola (T.d.) und Tannerella forsythia (T.f.). Gegen fakultativ anaerobe Keime wie Aggregatibacter actinomycetemcomitans (A.a.) hat Metronidazol allein aber kaum Wirkung – A.a. zeigt regelmäßig hohe minimale Hemmkonzentrationen gegenüber Metronidazol. Genau diese Lücke schließt Amoxicillin mit seinem breiteren Wirkspektrum.
Studien zeigten, dass Amoxicillin plus Metronidazol als Ergänzung signifikant bessere Ergebnisse bei der Reduktion tiefer Taschen erzielte als die klassischen Parodontosebehandlung allein.
Unter Amoxicillin/Metronidazol-Therapie konnten A.a. fast komplett elimineirt werden, was mit mechanischer Therapie allein nicht erreichbar war.
Das Wirkspektrum von Amoxicillin gegen Parodontitis-Leitkeime
Nicht jedes Antibiotikum wirkt gegen jeden Parodontitis-Erreger. Die folgende Übersicht zeigt, wo Amoxicillin seine Stärken hat – und wo es auf die Ergänzung durch Metronidazol angewiesen ist.
| Erreger | Komplex | Amoxicillin allein | Kombination mit Metronidazol |
|---|---|---|---|
| A. actinomycetemcomitans (A.a.) | – (eigene Rolle) | gut wirksam | sehr gut wirksam |
| P. gingivalis (P.g.) | Roter Komplex | begrenzt wirksam | sehr gut wirksam |
| T. denticola (T.d.) | Roter Komplex | begrenzt wirksam | sehr gut wirksam |
| T. forsythia (T.f.) | Roter Komplex | begrenzt wirksam | gut wirksam |
| P. intermedia (P.i.) | Oranger Komplex | mäßig wirksam* | gut wirksam |
| F. nucleatum (F.n.) | Oranger Komplex | teilweise wirksam* | gut wirksam |
Wann wird Amoxicillin bei Parodontitis eingesetzt, wann ist es unnötig?
Nicht jede Parodontitis braucht ein Antibiotikum – und die Leitlinie ist hier bewusst restriktiv. Antibiotika wirken systemisch: Sie belasten die Darmflora, können Nebenwirkungen verursachen und tragen bei unkritischem Einsatz zur Resistenzentwicklung bei. Daten aus deutschen Parodontologiepraxen zeigen, dass einzelne Stämme von A.a. und P. gingivalis bereits Resistenzen gegen gängige Antibiotika aufweisen. Die Kombination Amoxicillin/Metronidazol zeigt bislang erfreulich niedrige Resistenzraten – aber nur, solange sie gezielt und nicht inflationär eingesetzt wird.
Die S3-Leitlinie der DG PARO/DGZMK (2018) formuliert deshalb klare Kriterien für den adjuvanten Einsatz:
Indikationskriterien der S3-Leitlinie:
| Kriterium | Schwellenwert |
|---|---|
| Patientenalter | unter 56 Jahre |
| Erkrankungsausmaß | mehr als 35 % aller Messstellen mit TST ≥ 5 mm |
| Erkrankungsschwere | Stadium III (fortgeschrittene Parodontitis) |
Entscheidend: Diese Kriterien greifen als Kombination – nicht als unabhängige Einzelpunkte. Ein 60-Jähriger mit Stadium III erhält nach der Leitlinie primär keine Antibiose. Und auch bei Erfüllung aller Kriterien gilt: Das Antibiotikum kommt erst nach der mechanischen Therapie, nie als Ersatz dafür.
In der klinischen Praxis sehen viele Parodontologen zusätzliche Situationen, in denen eine adjuvante Antibiose sinnvoll sein kann – etwa bei nachgewiesenem A.a.-Befall im Bakterientest, bei rasch fortschreitenden Verläufen (Grad C) oder bei unzureichendem Ansprechen auf die mechanische Ersttherapie. Einen mikrobiologischen Test als Voraussetzung für die Antibiotikagabe fordert die Leitlinie allerdings nicht – die Empfehlung ist primär empirisch.
Für Patienten bedeutet das: Wenn Ihr Zahnarzt nach dem Scaling kein Antibiotikum verschreibt, ist das kein Versäumnis – sondern in den meisten Fällen die leitliniengerechte Entscheidung.
Dosierung nach Leitlinie:
| Wirkstoff | Dosierung | Häufigkeit | Dauer |
|---|---|---|---|
| Amoxicillin | 500 mg | 3× täglich | 7 Tage |
| Metronidazol | 400 mg | 3× täglich | 7 Tage |
Beide Präparate werden zeitgleich eingenommen, idealerweise zu den Mahlzeiten. Die Einnahme beginnt am Tag der letzten Scaling-Sitzung oder unmittelbar danach – nicht Tage oder Wochen später.
Amoxicillin bei Kieferinfektionen
Neben der Parodontitistherapie ist Amoxicillin das wichtigste Antibiotikum bei akuten odontogenen Infektionen – also bei Infektionen, die von Zähnen oder dem Zahnhalteapparat ausgehen. Dazu gehören:
- Akuter Wurzelabszess (periapikaler Abszess): Die häufigste Kieferinfektion überhaupt. Bakterien aus dem nekrotischen Zahnmark breiten sich über die Wurzelspitze in den umgebenden Knochen aus.
- Parodontalabszess: Eine akute Eiteransammlung in einer tiefen Zahnfleischtasche, oft bei vorbestehender Parodontitis.
- Dentogene Weichteilinfektion und Logenabszess: Wenn sich die Infektion über den Knochen hinaus in die umgebenden Weichgewebe ausbreitet – im Extremfall bis in den Mundboden (Angina Ludovici) oder den Augenbereich. Diese Fälle sind Notfälle.
- Perikoronitis: Entzündung des Zahnfleischs über einem teilweise durchgebrochenen Weisheitszahn.
- Postoperative Infektion nach Zahnentfernung oder Implantation.
β-Laktamase-Hemmer verbessert die Wirksamkeit von Amoxicillin
Viele Bakterien haben über die Zeit eine wirksame Gegenwaffe entwickelt: Sie produzieren Enzyme namens β-Laktamasen, die den β-Laktam-Ring des Amoxicillin-Moleküls aufbrechen – und damit das Antibiotikum zerstören, bevor es wirken kann. In der Mundhöhle sind es vor allem bestimmte Prevotella-Stämme und einige Fusobacterium-Isolate, die β-Laktamasen produzieren. Diese Bakterien können Amoxicillin nicht nur für sich selbst unwirksam machen, sondern schützen auch ihre Nachbarn im Biofilm mit – ein Phänomen, das als „indirekter Schutz“ oder „Bystander Protection“ bekannt ist.
Die Zahnmedizin kennt zwei Strategien, um dieses Problem zu umgehen:
Bei Parodontitis: Metronidazol als Partner.
Metronidazol wirkt über einen völlig anderen Mechanismus (DNA-Schädigung in anaeroben Zellen), der von β-Laktamasen nicht beeinflusst wird. Die Kombination Amoxicillin/Metronidazol umgeht das Problem also elegant: Metronidazol ist nicht nur synergistisch gegen Anaerobier, sondern gleichzeitig immun gegen die Abwehrstrategie der β-Laktamase-Bildner.
Bei Kieferinfektionen: Clavulansäure als Schutzschild.
Clavulansäure hat selbst kaum antibiotische Wirkung, blockiert aber gezielt die β-Laktamasen und stellt so die volle Wirksamkeit von Amoxicillin wieder her. Die Kombination wird als Amoxicillin/Clavulansäure vermarktet (Augmentin®, Amoxiclav). Bei unkomplizierten Infektionen ohne Ausbreitungstendenz – etwa im Frühstadium eines Abszesses, wenn die Infektion noch auf den Knochen begrenzt ist – reicht Amoxicillin allein (z. B. 3× 500 mg bis 3× 1000 mg) häufig aus. Sobald aber eine fortgeschrittene Mischinfektion mit hohem Anaerobieranteil vorliegt, empfiehlt die S3-Leitlinie der DGZMK (2016) Amoxicillin/Clavulansäure als Mittel der Wahl (z. B. 2× 875/125 mg oder 3× 625 mg). Alternative bei Penicillinallergie: Clindamycin – das allerdings wegen steigender Resistenzraten und des C.-difficile-Risikos zunehmend kritisch gesehen wird.
Was muss man bei der Einnahme von Amoxicillin bzw. des van-Winkelhoff-Cocktail beachten?
Wer die Diagnose „schwere Parodontitis mit Antibiotika-Indikation“ bekommt, hat verständlicherweise Fragen. Der typische Ablauf sieht so aus:
1. Erst die mechanische Therapie: Der Biofilm in den Zahnfleischtaschen wird durch Scaling und Wurzelglättung aufgebrochen. Ohne diesen Schritt können Antibiotika die im Biofilm geschützten Bakterien nicht erreichen – die Tabletten allein wären wenig effektiv.
2. Dann das Antibiotikum: Am Tag der letzten Scaling-Sitzung oder am Folgetag beginnt die 7-tägige Einnahme von Amoxicillin und Metronidazol. Die Bakterien sind jetzt aus dem schützenden Biofilm herausgelöst und für das Antibiotikum angreifbar.
3. Vollständig einnehmen: Auch wenn sich das Zahnfleisch nach drei oder vier Tagen schon besser anfühlt – die vollen sieben Tage sind wichtig. Ein vorzeitiger Abbruch begünstigt die Selektion resistenter Keime.
4. Alkohol meiden: Metronidazol und Alkohol vertragen sich nicht. Die Kombination kann Übelkeit, Erbrechen, Kopfschmerzen und Kreislaufprobleme auslösen (sogenannte Disulfiram-ähnliche Reaktion). Während der Einnahme und bis 48 Stunden danach sollte kein Alkohol getrunken werden.
ich habe eine Penicillinallergie – was nun?
Etwa 1–10 Prozent der Bevölkerung geben an, eine Penicillinallergie zu haben. Tatsächlich bestätigt sich diese bei allergologischer Testung nur bei einem Bruchteil der Fälle. Trotzdem muss eine dokumentierte Allergie ernst genommen werden.
Bei Parodontitis empfiehlt die Leitlinie bei gesicherter Penicillinunverträglichkeit die alleinige Gabe von Metronidazol (400 mg, 3× täglich, 7 Tage) als Alternative. Das ist die offizielle Zweitwahl – sie erfasst die strikt anaeroben Keime des roten Komplexes, hat aber Lücken bei A.a.
Bei Kieferinfektionen war Clindamycin die klassische Ausweichoption, wird aber wegen steigender Resistenzraten, gungünstigem Wirkspektrum und des Risikos einer Clostridioides-difficile-Infektion sehr kritisch bewertet. Alternativen sind je nach Situation Moxifloxacin oder die Kombination aus Metronidazol mit einem Makrolid (z.B. Azithromycin).
Mehr zur Antibiotikatherapie bei Parodontitis.
Was kostet Amoxicillin?
Amoxicillin gehört zu den preiswertesten Antibiotika weltweit. Das Originalpatent von Beecham ist längst abgelaufen – der Wirkstoff wird von zahlreichen Herstellern als Generikum produziert.
In Deutschland kostet ein 7-tägiger Behandlungskurs (Amoxicillin 500 mg, 21 Tabletten) in der Apotheke zwischen 5 und 12 Euro. Die gesetzlichen Krankenkassen erstatten die Kosten vollständig – es fällt lediglich die Rezeptgebühr von 5 Euro an. Zusammen mit Metronidazol (ebenfalls ca. 5–10 Euro) liegen die Gesamtkosten der Antibiotikatherapie bei unter 25 Euro. Amoxicillin/Clavulansäure ist etwas teurer (ca. 15–25 Euro), wird aber ebenfalls von der GKV erstattet.
| Amoxicillin | 500 mg, 7-Tage-Kurs |
|---|---|
| Indien | 1–2 € |
| Deutschland (Kassenrezept) | 5 € Zuzahlung |
| Deutschland (Privatrezept) | 14–18 € |
| Österreich | 6–10 € |
| Schweiz | 12–18 CHF |
| USA | 10–30 USD (ohne Versicherung) |
Im internationalen Vergleich zeigt sich: Amoxicillin ist überall ein preiswertes Medikament. Im Herstellungsland Indien kostet es fast gar nichts. Kosten sind also kein Hindernis für die Behandlung.
implantate.com-Fazit:
Amoxicillin ist in der Zahnmedizin ein Arbeitstier: Bei schwerer Parodontitis – in Kombination mit Metronidazol – das Mittel der Wahl, wenn die Leitlinienkriterien erfüllt sind. Bei Kieferinfektionen – allein oder mit Clavulansäure – das am häufigsten eingesetzte Antibiotikum. Es ist gut verträglich, preiswert und seit Jahrzehnten klinisch erprobt.
Behandlungsrichtlinie zur systematischen Behandlung von Parodontitis und anderer Parodontalerkrankungen (PAR-Richtlinie). In Kraft seit 01.07.2021.
Macy E, Romano A, Khan D: Practical management of antibiotic hypersensitivity in 2017. J Allergy Clin Immunol Pract 2017;5(3):577–586.
Al-Nawas B, komplett: S3-Leitlinie Odontogene Infektionen. AWMF-Registernummer 007-006, Deutsche Gesellschaft für Mund-, Kiefer- und Gesichtschirurgie (DGMKG), 2016.
Brook I: Microbiology and management of endodontic infections in children. J Clin Pediatr Dent 2003;28(1):13–17.
Baumgartner JC, Xia T: Antibiotic susceptibility of bacteria associated with endodontic abscesses. J Endod 2003;29(1):44–47.
GKV-Arzneimittelindex, Wissenschaftliches Institut der AOK (WIdO), 2023.